近日,信达生物传来好消息,其自研眼科新药——替妥尤单抗N01注射液(IBI311)获批上市,商品名:信必敏。这是中国首个、全球第二个IGF-1R抗体药物,用于治疗甲状腺眼病(Thyroid Eye Disease,TED)。
这也是信达生物今年首个获批的重磅新药,同时,公司另两款备受瞩目的潜在重磅产品——玛仕度肽和匹康奇拜单抗也有望在今年获批上市,开启非肿瘤领域快速增长通道。
01中国首个
甲状腺眼病(TED)也被称为GRAVES眼病,是一种与甲状腺疾病密切相关的自身免疫性疾病。据统计,约有25%-50%的弥漫性甲状腺肿伴甲亢患者会伴有不同程度的GRAVES眼病,位居成人眼眶疾病发病率首位。而且近年来该疾病呈现明显的年轻化趋势。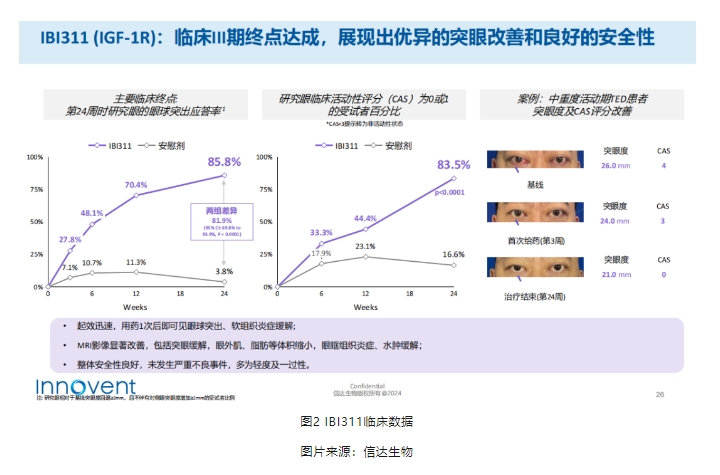
02开启增长“新引擎”
过去几年,信达生物在肿瘤领域通过自研与合作并举,打造了丰富管线矩阵。
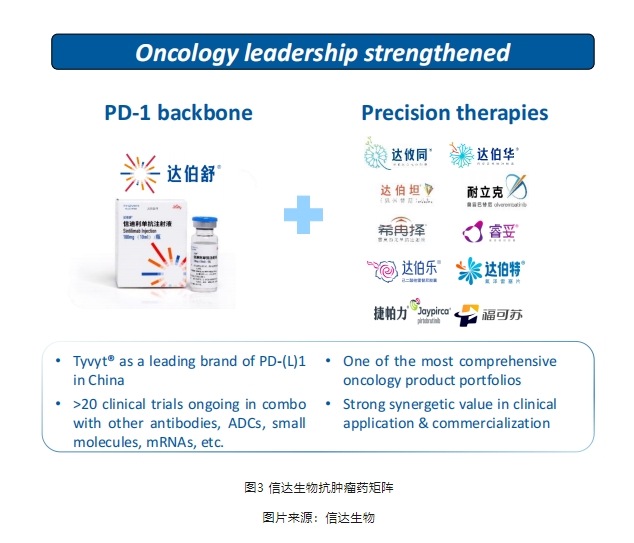
而在下一代抗肿瘤药物开发上,信达生物采取“IO+ADC”战略,布局了联合疗法(CTLA-4单抗+信迪利单抗),新一代ADC药物:IBI354(HER2 ADC)、IBI3009(DLL3 ADC)、IBI343(CLDN18.2 ADC),双抗药物:IBI363(PD-1/IL-2α-bias)等众多潜力管线。
不过,这些抗肿瘤药物大多面临激烈竞争,或者还处于临床早期。从目前的布局来看,信达生物下一个“重磅炸弹”很可能在非肿瘤领域。
刚刚获批上市的甲状腺眼病新药IBI311即是一个潜在重磅产品。除此之外,信达生物今年还有两个非肿瘤重磅新药有望获批上市:玛仕度肽和匹康奇拜单抗。
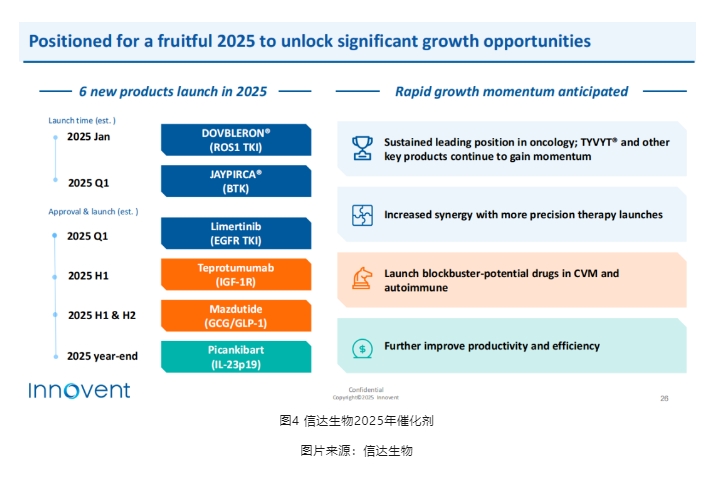
玛仕度肽
全球GLP-1药物的热度有目共睹。而在国内,信达生物占得先机。
玛仕度肽是信达生物从礼来引进的一款GCGR/GLP-1R双重激动剂。其中GLP-1受体激动剂主要作用在于抑制食欲、延缓胃排空、减少能量摄入。而GCG受体激动剂对于机体脂肪代谢具有重要调节作用:一方面抑制脂肪合成,一方面促进脂肪分解,增加能量消耗,起到1+1>2的协同作用。因此,玛仕度肽在减重效果上有超越司美格鲁肽的潜力。
其针对中国超重患者的Ⅲ期GLORY-1研究显示,32周时,4mg和6mg剂量组的受试者体重较基线分别下降10.54%和13%(安慰剂校正后数据)。48周时,4mg和6mg组体重较基线分别下降11.3%和14.31%(安慰剂校正后数据)。
在安全性方面,4mg、6mg和安慰剂组的严重不良事件发生率分别为4.4%、3.5%和6.3%;因不良事件停药的比例分别为1.5%、0.5%和1.0%。
针对全球超重或肥胖患者的I期临床研究显示,高剂量16mg玛仕度肽20周减重最高达21%,而安慰剂组几乎没有变化(-0.1%)。主要不良事件为轻中度恶心、呕吐和腹泻,未观察到严重不良事件。
此外,玛仕度肽还具有独特的肝脏获益、改善肥胖相关炎症等作用。目前,该药用于体重管理和成人2型糖尿病两项适应症均已提交上市申请,信达生物预计这两项适应症分别将在2025年上半年和下半年获批上市。
匹康奇拜单抗
自免是另一个“大药”市场。
信达生物的匹康奇拜单抗(IBI112)已在去年递交上市申请,适应症为中重度斑块状银屑病,预计将在今年年底获批上市。
该药是一款IL-23p19单抗,具有同类最佳疗效潜力和长间隔给药。
据信达新闻稿,匹康奇拜单抗是全球首个注册Ⅲ期临床首要研究终点中第16周达到PASI 90的受试者比例突破80%的IL-23p19抗体药物,同时在同类生物药中具有最长的维持期给药间隔(每12周一次)。
CLEAR-1研究显示,第16周达到PASI 90和sPGA 0/1的受试者比例分别达到80.3%和93.5%。第16周达到PASI 75、PASI 100、sPGA 0、DLQI 0/1的受试者比例显著高于安慰剂。
另外,匹康奇拜单抗治疗溃疡性结肠炎的Ⅱ期临床研究也达成了主要终点。
除了这几款今年有望上市的新药,信达生物在非肿瘤领域还有多个在研管线,包括:
IBI302:该药是一款抗VEGF-抗补体双特异性重组全人源融合蛋白,展现出非劣于阿柏西普的视力获益、更长给药间隔下的疗效持久性和黄斑萎缩改善的潜力。目前IBI302 8mg治疗nAMD的3期临床试验STAR患者招募入组进行中。
IBI128:替古索司他片,该药是信达生物从韩国LG化学引进的一款非嘌呤类似物——黄嘌呤氧化酶抑制剂(XOI),目前在中国进行2期临床研究。未来,非肿瘤领域(眼科、心血管和代谢、自免)或将成为信达新的重要收入来源。
03稳步迈向200亿目标
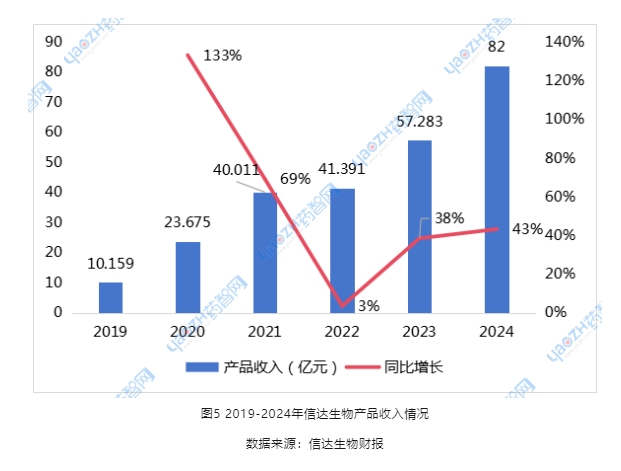
2022年,信达生物喊出“2027年国内产品收入达到200亿元”的目标。根据信达公告,2024年信达产品收入已超过82亿元,同比增速40%以上。而今年信达生物有望增加多个“爆款”产品,推动业绩快速增长,实现200亿目标指日可待。