概述
富马酸伏诺拉生片(vonoprazan Fumarate,TAK-438)由日本武田(Takeda)制药和大冢制药联合开发,2015年2月获日本劳动卫生福利部(MHLW)批准上市,用于治疗糜烂性食管炎、胃溃疡、十二指肠溃疡、幽门螺杆菌根除适应症。本品为一种新型的钾离子竞争性酸阻滞剂(P-CABs),该药可以在不依赖酸性环境的情况下,以钾离子竞争性的方式可逆性的抑制胃壁细胞上H+/K+-ATP酶,强酸性环境中较为稳定,可迅速、强效、持久的抑制胃壁细胞分泌胃酸,显著降低夜间胃酸升高的发生。
参比制剂国内上市情况:2018年3月我国国家药品监督管理局药品评审中心正式受理了沃克(富马酸伏诺拉生片)的上市申请。2019年12月18日富马酸伏诺拉生在我国正式批准上市,用于治疗反流性食管炎,也成为了首款进入中国的钾离子竞争性酸阻滞剂(P-CABs)。其适应症为反流性食管炎及与适当的抗生素联用以根除幽门螺杆菌。2020年底,伏诺拉生成功进入国家医保药品目录。目前原研已申报地产化,受理号为CYHS2404094,持有人为天津武田药品有限公司,目前待审评。
药典收载情况:本品原料药及制剂尚未收入ChP2020、BP、USP及JP。
参比制剂情况:国家公布的参比制剂信息如下:
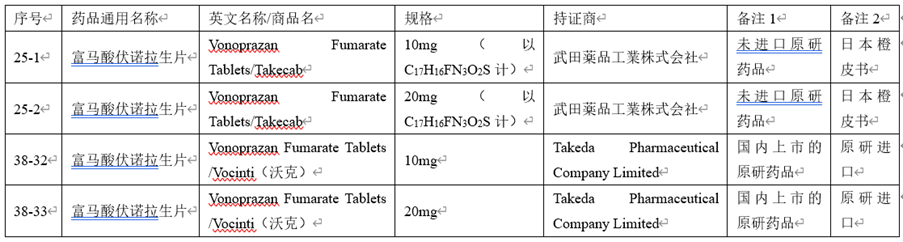
仿制药国内上市情况
目前该片剂在CDE官网上已有188个受理号(还有多家制剂等待审评),目前国内上市的富马酸伏诺拉生片仿制药有8家,具体如下:
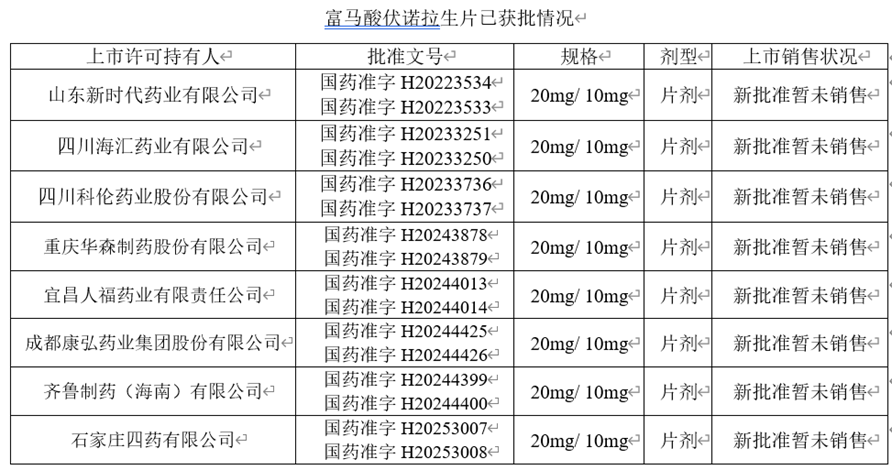
登记备案平台有55家企业已进行原料药登记备案,还有多家原料药正在审评中。原料药的获批情况如下所示:
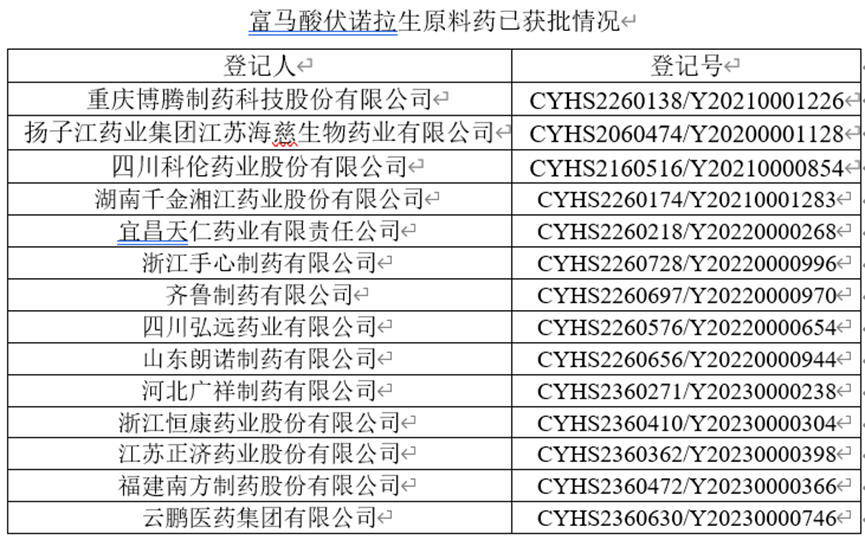
3、富马酸伏诺拉生缘何如此“卷”这个产品的仿制缘何如此“卷”,下表汇总了该产品与质子泵抑制剂的药学特性对比,该数据来自中国药房公众号。
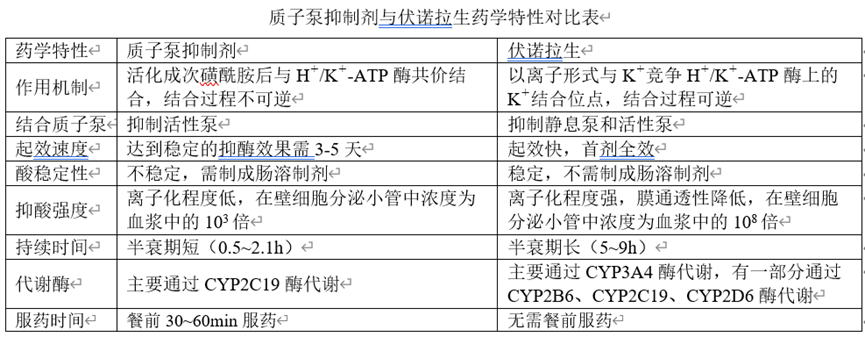
伏诺拉生是新一类胃酸分泌抑制剂,通过竞争性抑制K+对质子泵的结合作用,提前终止胃酸的分泌,起效迅速,其作用强劲、持久,且无需酸激活。大量的临床前药理毒理评价表明本品具有良好的药效和较高的安全性。在临床试验中,相对于PPIs,本品的疗效更佳,而安全性相似。本品的优点还在于服用方便,不受胃酸影响,无需优化配方设计,患者个体起效剂量差异不显著。本品可改善夜间酸突破现象,与目前上市的同类药物瑞伐拉赞相比,使用剂量更低。因此本品有望成为一种新的治疗药物,以解决当前酸相关疾病治疗中存在的问题。且本品目前原研独占市场,市场潜力大。
本品仿制关注点
为促进本品的成功仿制,结合前期文献调研及实际研发经验,对本品仿制过程中的关注点进行论述,以期对业界有一定的启示作用。刻痕片:原研有2个规格(10mg和20mg),20mg有双面刻痕。说明书相关描述显示该刻痕可能是非功能性刻痕,故可能不需要严格按照功能性刻痕的相关要求进行研究。BE豁免:关于大小规格BE豁免需满足相应指南要求,处方相似,溶出曲线在指导原则要求的溶出介质中均应相似,即需要符合《以药动学参数为终点评价指标的化学药物仿制药人体生物等效性研究技术指导原则》要求。亚硝胺杂质:FDA官网于2021-11-18报道了《降低药品中亚硝胺药物成分相关杂质风险的缓解策略》一文,其中提到关于辅料与API形成API结构相似亚硝胺杂质(NDSRIs),相关文献显示,有引入亚硝酸风险的辅料种类包括羧甲基纤维素钠、乳糖、预胶化淀粉、微晶纤维素等。本品含有仲胺基团,且处方中可能会用到以上辅料,有引入亚硝胺杂质的风险。需关注并研究,拟定合理的控制限度,考虑订入注册标准。专利情况:原料药专利于2026年过期,需关注是否存在专利侵权问题,目前获批上市的相关产品均不能上市销售。
本文通过前期文献调研,以期对新一代强效阻酸剂进行较为详细的介绍,为后续业界进行本品的研发及注册申报提供启示,助力该产品的顺利获批。
参考文献
富马酸伏诺拉生的相关专利信息
日本IF文件
FDA官网相关文献资料
来源:药事纵横。如有侵权,联系立删。